
Retinopatia diabetica: risultati incoraggianti per una prima terapia orale
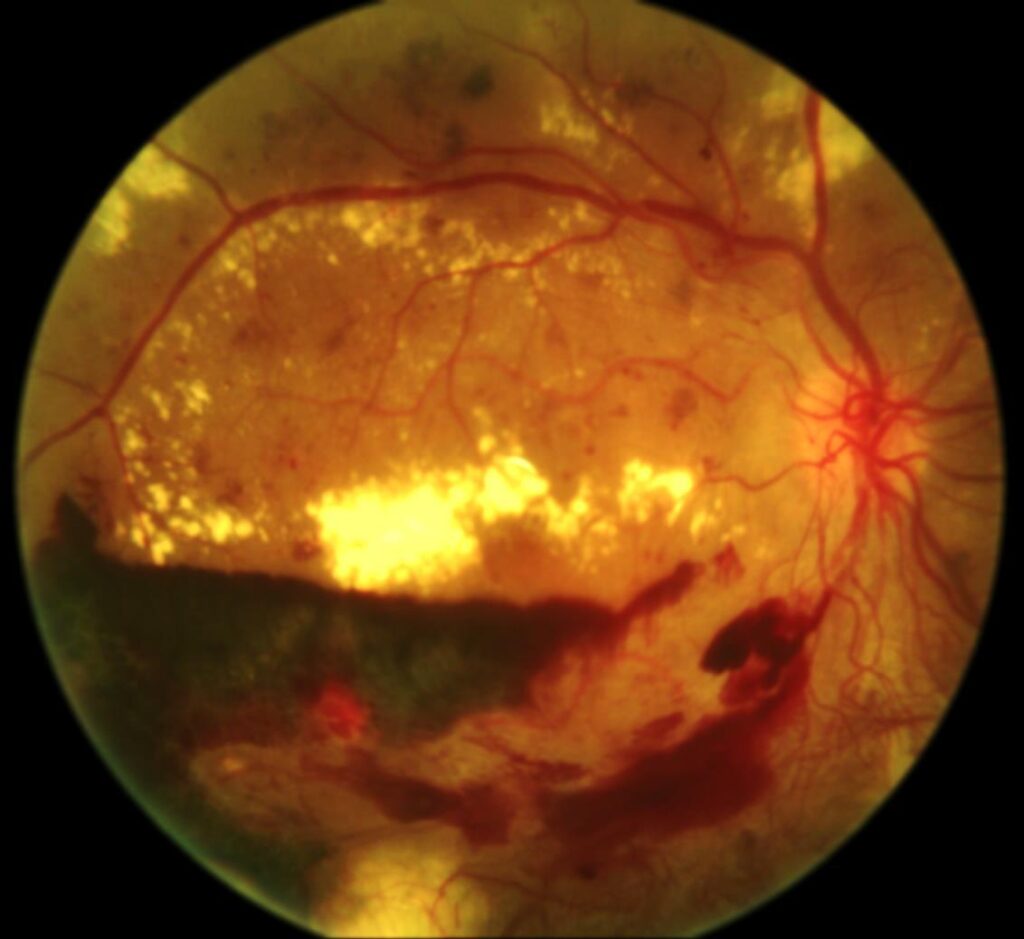
Nella ricerca il candidato APX3330 orale ha dimostrato di non raggiungere l’endpoint primario ma di bloccarsi all’endpoit secondario, punto cruciale per l’avanzamento della malattia, secondo quanto riportato dalla biotech Ocuphire Pharma.
La crescente crescita del diabete a livello mondiale e i rischi collegati a questo tipo di malattia, accrescono la necessità di cercare rimedi per gli effetti collaterali che essa può comportare, proprio come la retinopatia diabetica. «I pazienti diabetici con retinopatia non proliferativa hanno opzioni terapeutiche limitate per prevenire la progressione della malattia e la perdita della vista» ha osservato Peter Kaiser, professore di oftalmologia presso il Cole Eye Institute della Cleveland Clinic Foundation.
il profilo favorevole che ha mostrato APX3330 orale potrebbe portare l’accesso al farmaco a tutti gli operatori sanitari, e ai pazienti in fase non acuta della malattia di poterne usufruire prima che essa degeneri. In più ha il vantaggio di essere un farmaco, un agente oculare, che va a trattare entrambi gli occhi contemporaneamente e non uno solo.
Durante lo studio i partecipanti sono stati randomizzati a ricevere 600 mg di APX3330 o placebo due volte al giorno per 24 settimane. Gli endpoint primari e secondari valutati erano in miglioramento e peggioramento di +/- 1, 2, 3 e 4 gradi nel DRSS alla settimana 12 e alla settimana 24, la variazione dell’acuità visiva con la migliore correzione (BCVA), la variazione dello spessore del sottocampo centrale (CST), la sicurezza e la tollerabilità. I dati demografici dei pazienti e le caratteristiche basali erano ben bilanciati in entrambi i gruppi di trattamento. Inoltre APX3330 ha dimostrato di non avere ripercussioni sulle funzioni renali, cardiache o epatiche.
APX3330 non ha raggiunto l’endpoint primario relativo alla percentuale di pazienti con un miglioramento almeno 2 gradi nel DRSS alla settimana 24 nell’occhio studiato. Nessun paziente (0%) in trattamento attivo ha infatti avuto un peggioramento binoculare almeno 3 gradi del DRSS rispetto al basale in confronto al 16% del gruppo placebo (p=0,04)
APX3330 ha mostrato buon profilo di sicurezza e tollerabilità. Gli eventi avversi correlati al trattamento erano rari e di gravità lieve, non sono stati osservati eventi avversi correlati al trattamento e variazioni nelle funzionalità.
